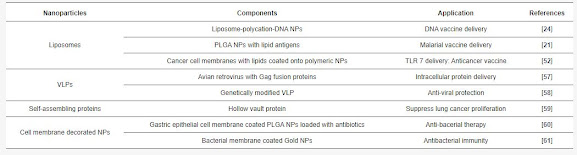
Jenis Biomimetic Nanoparticles (Nps)
Tabel menjelaskan berbagai jenis vaksin nano biomimetik yang dilaporkan sejauh ini beserta aplikasinya.
Liposom
Liposom adalah produk biomimetik yang dibentuk dengan mendispersikan fosfolipid dalam air. Mereka terjadi baik sebagai vesikel unilamellar dengan bilayer fosfolipid tunggal, atau sebagai vesikel multilamelar dengan beberapa cangkang fosfolipid konsentris dipisahkan oleh lapisan air yang berbeda. Liposom dapat dimodifikasi untuk menggabungkan molekul hidrofobik dan hidrofilik ke dalam lapisan ganda fosfolipid dan inti berair. Liposom dapat digunakan untuk mengenkapsulasi antigen di dalam intinya untuk pengiriman. Mereka membentuk virosom ketika glikoprotein envelope virus dimasukkan ke dalam basis mereka. Virus influenza adalah fokus utama untuk studi virosom yang telah ditetapkan untuk aplikasi industri sebagai vaksin manusia. Lima vaksin berdasarkan virosom sedang dalam uji klinis, dan empat vaksin virosom disetujui untuk aplikasi komersial pada berbagai penyakit. Salah satu NP yang umum digunakan untuk pengiriman adjuvant dalam vaksin DNA adalah NP liposom-polikasi-DNA; mereka dibentuk oleh kombinasi liposom kationik dan DNA terkondensasi polimer kationik. Liposom-polikasi-DNA berkumpul untuk membentuk struktur nano, dengan DNA terkondensasi terletak di dalam liposom dengan ukuran 150 nm. Bulan dkk. melaporkan pengembangan vaksin malaria, yang dapat digunakan untuk pengiriman NP PLGA polimer yang diselimuti dengan antigen lipid. Dalam pekerjaan mereka, Moon dan rekan kerja mengembangkan nanovaccine yang pathogen-mimicking, di mana kandidat antigen malaria dikonjugasikan ke membran lipid dan digabungkan dengan molekul imunostimulator, monofosforil lipid A-MPLA, dan selanjutnya digunakan untuk memperoleh respons imun terhadap P. vivax sporozoit. Yang dkk. menggunakan membran sel kanker yang dimodifikasi dengan lipid menggunakan metode penahan lipid, dan kemudian melapisinya lebih lanjut di atas NP polimer dengan toll-like receptor 7 (TLR 7). Nanocarrier membran biomimetik ini dilaporkan untuk digunakan sebagai vaksin antikanker, serta untuk pengiriman TLR 7 sebagai adjuvant.
Virus-Like Particles (VLPs)
VLP adalah molekul yang menyerupai struktur virus tanpa
materi genetik virus. NP self-assembling yang kekurangan asam nukleat ini
dibentuk oleh self-assembly protein kapsid biokompatibel. Mereka adalah sistem
nanovaksin yang ideal, karena mereka memiliki struktur virus bawaan, yang dapat
berinteraksi dengan sistem kekebalan tubuh tanpa ancaman menyebabkan infeksi.
VLP ini dapat bertindak sebagai vaksin yang memiliki ukuran nano dan urutan
struktural yang berulang, dan dapat menginduksi respon imun tanpa adanya
adjuvant. VLP berkumpul tanpa merangkum RNA virus apa pun, dan karenanya mereka
tidak menular dan tidak bereplikasi, karena gen yang dikodekan untuk integrase
virus dihapus sebelum ekspresi. Ini mencegah integrasi genom yang dikemas ke
dalam sel inang, serta rekombinasi virus hidup atau yang rusak. Vaksin VLP
pertama dikembangkan untuk melawan virus hepatitis B, yang kemudian
dikomersialkan pada tahun 1986. Vaksin VLP terhadap hepatitis E dan human
papillomavirus telah digunakan pada manusia sejak tahun 2006.
VLP dapat diperoleh dari berbagai virus, dan dapat memiliki
ukuran yang berbeda mulai (20 hingga 800) nm; lebih lanjut, mereka dapat
diperoleh melalui proses yang berbeda. Pendekatan awal untuk mendapatkan VLP
melibatkan self-assembly protein kapsid dalam host ekspresi, diikuti dengan
pemurnian protein yang diasembly untuk menghindari kontaminan yang melekat atau
dienkapsulasi. Namun, dalam beberapa kasus, untuk kualitas yang lebih baik dan
kontaminasi yang rendah, struktur VLP perlu dibongkar dan dipasang kembali.
Metode lain yang muncul untuk mendapatkan VLP adalah dengan menggunakan
pemrosesan in vitro bebas sel, di mana pada awalnya pemurnian skala besar
dilakukan untuk mencegah kontaminasi, dan kemudian perakitan struktur VLP in
vitro, untuk menghindari pembongkarannya dalam sel; VLP yang dikomersialkan
berasal dari virus target dengan self-assembly proteinnya.
Agar VLP digunakan sebagai sarana pengiriman, antigen target dari virus yang berbeda dari yang digunakan dalam VLP dilekatkan pada permukaan VLP; dan VLP yang dimodifikasi permukaan ini membuka jalan untuk penggunaannya dalam menargetkan berbagai penyakit. VLP dapat direkayasa untuk menempelkan protein tambahan pada permukaannya, baik melalui fusi protein pada partikel, atau dengan mengekspresikan beberapa antigen, yang pada gilirannya melindungi terhadap virus sumbernya dan antigen lain yang ada di permukaannya. Polisakarida dan molekul organik kecil merupakan antigen non-protein yang secara kimiawi dapat melekat pada permukaan VLP untuk membentuk partikel biokonjugasi. Sistem ekspresi baculovirus sebagian besar digunakan untuk menghasilkan VLP dengan profil keamanan yang sangat baik, karena baculovirus tidak menginfeksi manusia secara alami. Dalam studi lain, sistem VLP yang aman dan efisien berdasarkan retrovirus unggas dirancang sedemikian rupa sehingga sistem dianggap aman, karena tidak dapat mereplikasi dirinya sendiri dalam sel manusia. Sistem ini dianggap aman karena VLP hanya merupakan protein fusi Gag; satu VLP dapat mengirimkan sekitar (2000-5000) salinan protein fusi Gag ke dalam sel yang ditransduksi. Dalam studi lain, VLP dibuat untuk pengiriman dengan dua pendekatan berbeda: distribusi intraseluler protein fusi Gag, atau dengan memodifikasi permukaan VLP untuk pengiriman yang dimediasi reseptor/ligan.
Gambar. Skema generasi partikel virus-like particle (VLP) dan (A) pengiriman protein yang menarik secara intraseluler, dan (B) oleh pengiriman protein yang diperantarai reseptor/ligan.Self-assembling Protein Nanoparticles (NPs)
Banyak protein alami dapat self-assembly untuk membentuk NP
dengan simetri dan stabilitas yang tinggi, dan NP ini secara struktural diatur
untuk membentuk partikel dengan ukuran berkisar (10-150) nm. NP ini dengan
peran fisiologis yang beragam dipilih sebagai pembawa vaksin, karena kemampuan
mereka untuk self-assembly dan menyebarkan ke dalam struktur tertentu yang
meniru arsitektur mikroba alami.
Feritin adalah protein yang melindungi sel dari kerusakan
yang disebabkan oleh reaksi Fenton, di mana besi mengkatalisis hidrogen
peroksida, dan mengubahnya menjadi radikal hidroksil yang sangat beracun. Dalam
kondisi pengoksidasi, spesies oksigen reaktif yang berbahaya dihasilkan dari
Fe(II) bebas, yang dapat merusak mesin seluler. Feritin memiliki struktur
berongga, dan kemampuan untuk menyimpan besi di dalam rongga berongga ini;
dengan demikian, ia bertindak sebagai sistem penyimpanan untuk besi. Feritin
dapat self-assembly menjadi struktur nano bulat dan digunakan untuk menyatu
dengan virus influenza haemagglutinin (HA) secara genetik, dan protein
rekombinasi secara spontan berkumpul menjadi partikel simetri oktahedral.
Reformasi ini menjadi delapan trimeric HA trimerik, dan memunculkan respon imun
yang lebih kuat, dibandingkan dengan virus influenza trivalen yang tidak aktif.
Jenis lain dari protein self-assembly adalah major vault protein (MVP). Juara
dkk. melaporkan bahwa 96 unit MVP self-assembly untuk membentuk NP barrel-shaped
dengan panjang 70 nm dan lebar 40 nm.
Lebih lanjut, mereka menyebutkan bahwa antigen yang menyatu
secara genetik yang memiliki interaksi minimal dapat dimuat ke NP vault yang
telah diself-assembly melalui pencampuran dengan MVP. Dalam pekerjaan mereka,
mereka mengenkapsulasi protein imunogenik yang disebut protein membran luar
utama Chlamydia muridarum ke dalam hollow vault nanocapsules. Hollow vault
nanocapsules ini dimodifikasi untuk mengikat IgG untuk meningkatkan respon
imun, untuk menginduksi imunitas protektif pada permukaan mukosa yang jauh.
Wahom dkk. melaporkan protein self-assembling lain NP, imunogen bebas adjuvant
yang diperoleh dengan self-assembly rantai monomer menjadi bentuk oligomer yang
dipesan sebagai sistem penyajian antigen yang cocok untuk vaksin. NP protein
yang self-assembly ini dibentuk dengan menggabungkan membrane-proximal external
regio (MPER) HIV-1 gp41, yang diidentifikasi sebagai target untuk berbagai
antibodi penetral, di pentamer terminal-N, untuk menghasilkan -keadaan heliks
epitop 4E10, tanpa menyebabkan perubahan struktural pada epitop 2F5. NP yang diself-assembly
ini menunjukkan peningkatan titer spesifik wilayah membran-proksimal, karena
adanya tampilan antigen berulang dari MPER bahkan tanpa bahan adjuvan, sehingga
menghasilkan pembentukan imunogen bebas bahan adjuvan sebagai vaksin HIV
potensial.
Cell Membrane-Decorated Nanoparticles (NPs)
Seperti yang dibahas pada bagian sebelumnya, NP yang
didekorasi dengan membran sel telah muncul sebagai metode yang menjanjikan
untuk kamuflase dengan membentuk lapisan tipis lapisan membran sel di atas NP.
NP yang disamarkan mewarisi sifat-sifat sel sumber, tergantung pada sel sumber
yang digunakan. Misalnya, ketika sel darah merah digunakan sebagai membran
sumber, NP berlapis membran ditemukan memiliki penghindaran imun dan sirkulasi
yang berkepanjangan. NP biomimetik mencapai sifat meniru sel ini dengan
pemindahan protein membran sel sumber ke permukaan NP. Pendekatan
fungsionalisasi ini dianggap sangat serbaguna, memungkinkan pengiriman berbagai
kargo yang mencakup berbagai bahan inti dalam.
Penghantaran obat yang ditargetkan menggunakan kemampuan
melekat yang melekat pada sel sumber. Misalnya, NP yang disamarkan dengan
lapisan membran sel kanker menunjukkan sifat adhesi homotipik yang diwariskan,
dan kapasitas intrinsik untuk mengikat dengan sel sumber. Selain itu, NP yang
disamarkan dengan membran trombosit menunjukkan kemampuan untuk meniru
pengikatan trombosit dengan patogen, seperti Staphylococcus aureus yang
resisten methicillin, untuk pengiriman antibiotik yang ditargetkan. Sementara
itu, trombosit membantu dalam mengenali sel tumor, termasuk sel tumor yang
bersirkulasi, melalui interaksi pengikatan ligan mereka. NP yang disamarkan
dengan membran trombosit terutama diformulasikan untuk pengiriman obat
antikanker spesifik lokasi. Aplikasi persuasif ini mengilhami pengembangan NP membran
sel yang disamarkan untuk pengiriman antibiotik yang ditargetkan terhadap
infeksi H. pylori. Angsantikul dkk. melaporkan nanoterapi yang diperoleh dengan
melapisi poli (asam laktat-co-glikolat) antibiotik (PLGA NP) dengan membran sel
epitel lambung terhadap infeksi H. pylori. Dalam studi mereka, ditemukan bahwa
NP berlapis membran sel epitel lambung memiliki antigen permukaan yang sama
dengan sel sumber yang menunjukkan adhesi yang melekat terhadap bakteri H.
pylori.
Penggunaan membran bakteri sebagai bahan vaksinasi telah
mendapatkan minat yang cukup besar. Mereka dapat merangsang kekebalan bawaan
dan mempromosikan respon imun adaptif dengan menunjukkan pathogen
associated-molecular patterns (PAMPs) untuk sejumlah besar antigen imunogenik
dengan sifat adjuvant. Penyamaran NP dengan menutupi membran bakteri
menghasilkan pelestarian karakteristik bakteri, dan dengan demikian membantu
dalam mimicking natural antigen alami oleh bakteri ke sistem kekebalan. Gao
dkk. melaporkan membran bakteri NP dilapisi untuk terapi antibakteri, di mana
NP emas dilapisi dengan vesikel luar bakteri. Dalam penelitian ini, mereka
memilih bakteri E. coli, memperoleh membran luarnya, dan melapisi NP emas
berukuran 30 nm dengan mereka; mereka menemukan bahwa ini dapat menginduksi
aktivasi cepat dan pematangan DC di kelenjar getah bening. Selanjutnya,
vaksinasi dengan NP ini menghasilkan respon antibodi yang tahan lama dan kuat.
Exosomes
Eksosom adalah vesikel ekstraseluler tertutup membran berukuran
nano yang berasal dari membran endosom bagian dalam. Vesikel ini terdiri dari
bilayer lipofilik dengan protein dan materi genetik seperti RNA mikro, mRNA,
dan DNA. Eksosom merupakan mediator antar sel dan dapat menginduksi respon imun
dengan mengaktifkan sel natural killer (NK), dendritic cells (DC), dan sel
limfosit T. Berbagai rangsangan fisiologis seperti peradangan, stres oksidatif
dan pertumbuhan sel mempengaruhi sekresi eksosom dari sel yang digunakan
sebagai penanda diagnosis yang menonjol. Eksosom bertindak sebagai vaksinasi
terhadap infeksi. Ini dapat digunakan sebagai pembawa antigen patogen dengan
memodulasi respon imun dan merekrut monosit, makrofag, sel NK, dan sel T
melawan agen infeksi.








No comments